本試卷分第Ⅰ卷(選擇題)和第Ⅱ卷(非選擇題)兩部分,滿150分.考試時間1 20分鐘.
選擇題
一、選擇題:本題共15小題,每小題4分,共60分.在每小題給出的四個選項中,只有一項是符合題目要求的.(成人高考更多完整資料免費提供加微信/QQ:29838818)
1.如圖2-1所示,一個光滑的小球,放在光滑的墻面和木板之間,木板與墻面之間的夾角為α.當α角增大時( )
A.墻對小球的彈力減小,木板對小球的彈力增大
B.墻對小球的彈力減小,木板對小球的彈力減小
C.墻對小球的彈力增大,木板對小球的彈力減小
D.墻對小球的彈力增大,木板對小球的彈力增大
2.有兩個質量相同的人造地球衛星,在半徑分別為R1、R2的圓周軌道上運動.它們所受向心力為F1、F2,運動速率為ν1、ν2,設R1
A.F1
B.F1>F2,ν1<ν2
C.F1
D.F1>F2,ν1>ν2
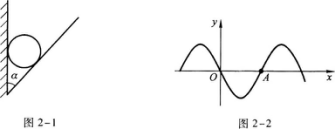
3.圖2-2是一個沿x軸正方向傳播的簡諧橫波在t=0時的波形圖,則A點的振動圖像是圖2-3中的( )(成人高考更多完整資料免費提供加微信/QQ:29838818)
A.(a)
B.(b)
C.(c)
D.(d)
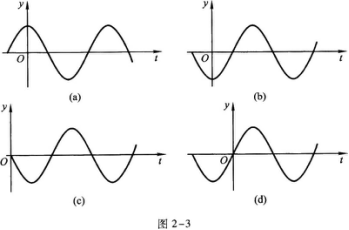
4.如圖2—4所示,R0為固定電阻,R為滑動變阻器,P為滑動變阻器的觸頭.當P滑動時,總電阻的變化是( )
A.當P向左滑時,總電阻減小
B.當P向右滑時,總電阻減小
C.P滑到最左端,總電阻等于R0
D.P滑到最右端,總電阻等于R0
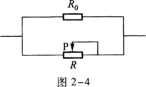
5.如圖2-5所示,在虛線范圍內有勻強磁場,磁場方向垂直紙面向里.已知矩形線圈abcd運動到圖示位置時,cd邊所受磁場力的方向豎直向上,則線圈的運動情形是( )
A.向左平動
B.向右平動
C.向上平動
D.向下平動
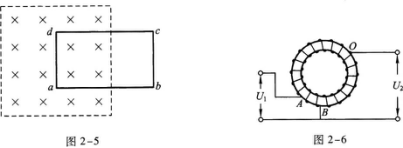
6.如圖2-6所示,從繞在鐵心上的線圈AB的0點引出一個抽頭,已知AO間的匝數為n1,BO間的匝數為n2.當BO間的交變電壓為U2時,AB間的交變電壓為( )
![]()
A.
![]()
B.
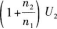
C.
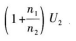
D.
7.放射性元素放出的三種射線中,貫穿本領最強和電離作用最強的射線分別是( )
A.β射線,α射線
B.γ射線,β射線
C.γ射線,α射線
D.α射線,β射線
8.下列物質中不能由金屬單質與非金屬單質直接反應制得的是( )
A.FeS
B.Cu2S
C.FeCl2
D.CuCl2
9.常溫下,下列溶液中可用鐵制容器盛裝的是( )
A.硫酸銅溶液
B.濃鹽酸
C.濃硫酸
D.稀硝酸
10.下列各組氣態氫化物中,其熱穩定性由大到小順序排列的是( )
A.HF、HCl、HI
B.NH3、H2O、HF
C.PH3、SiH、CH4
D.H2S、HCl、HBr
11.現有20 mL由兩種氣態烴組成的混合物,在足量的O2中完全燃燒,生成40 mLCO2和30 mL水蒸氣(在同溫同壓下測得).該混合物可能由下列哪兩種烴組成( )
A.C2H2、C2H4
B.C2H4、C2H6
C.CH4、C2H2
D.C2H4、C3H8

12.工業上制造金剛砂(SiC)的化學方程式為在此反應中還原劑和氧化劑的物質的量之比為( )(成人高考更多完整資料免費提供加微信/QQ:29838818)
A.1:2
B.2:1
C.1:3
D.3:1
13.在加壓或降溫條件下,下列可逆反應的平衡都向右移動的是( )
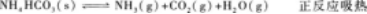
A.
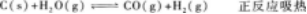
B.
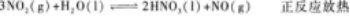
C.

D.
14.X、Y、Z三種元素的原子具有相同的電子層數,它們的最高價含氧酸的酸性強弱順序是H3XO4
A.原子序數X>Y>Z
B.原子半徑X
C.氣態氫化物的穩定性H3X>H2Y>HZ
D.元素的非金屬性X
15.一種鹽A跟KOH混合共熱,生成有刺激性氣味的氣體B.B經過一系列氧化后溶于水可得酸M,B與M反應又生成A.則鹽A是( )
A.NH4Cl
B.NH4NO3
C.(NH4)2SO4
D.(NH4)2CO3
非選擇題
二、填空題:16~19題每題6分,20~28題每空3分,共57分,把正確答案填在題中橫線上.
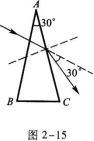
16.如圖2-7所示,三棱鏡ABC,∠A=30°.光線垂直AB面射人棱鏡,由AC面射出.已知出射光與入射光的夾角為30°.在AC面上光線的入射角是,棱鏡的折射率是.
17.如圖2—8所示,一個物體沿光滑的斜面從頂端由靜止開始下滑,斜面高h=10 m,斜面的傾角是30°物體滑到斜面中點的時間t=s,速率νm/s.(取g=10 m/s2.)
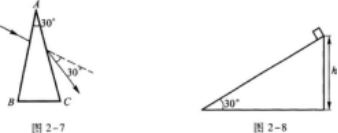
18.如圖2-9所示,勻強磁場的磁感應強度B=0.2 T,正方形線圈每邊長為0.1 m,通電流I=0.5 A,線圈所受磁場力大小是N,方向是.
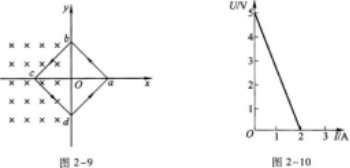
19.圖2-10是閉合電路的U-I曲線.由圖可知,閉合電路中電源的電動勢ξ=V,電源的內阻r=Ω.當路端電壓U=2.5 V時,外電阻R=Ω.
20.2,4-二甲基-4,5-二乙基庚烷的結構簡式為.
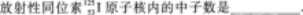
21.
22.充分燃燒2 mol某炔烴,消耗17 mol氧氣.該炔烴的分子式是.
23.等體積混合0.1 mol/L鹽酸和0.06 mol/L氫氧化鋇溶液,混合后溶液的pH=.

24.
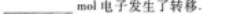
25.有機物X中含碳40%、氫6.7%、氧53.3%,其蒸氣密度是相同狀況下氧氣密度的0.938倍.X溶于水,水溶液呈中性,且具有還原性,可知X的結構簡式為.
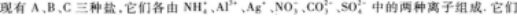
26.
都易溶于水,用其水溶液做如下實驗,實驗現象是:
(1)向3種溶液中分別加入鹽酸并加熱,A溶液與鹽酸不反應;B溶液有白色沉淀生成;C溶液則生成無色無味氣體.
(2)向A溶液中加入氫氧化鈉溶液,先生成白色沉淀,再繼續加氫氧化鈉溶液時,沉淀消失.
(3)向C溶液中加入過量氫氧化鈉溶液并加熱,產生一種有刺激性氣味的氣體.
根據以上現象,可判斷A為,C為.
27.化合物YX2和ZX2中,X、Y、Z三種元素位于周期表中前三周期,X與Y屬于同一周期,Y與Z是同主族元素.Y原子的核外電子層數與次外層電子數相等,最外層電子數是次外層電子數的2倍.X原子最外層電子數比次外層電子數多4個.Z元素的名稱是,YX2的分子式為.
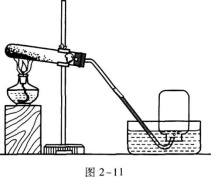
28.在實驗室內欲制取H2、O2、CO2、NH3、CH4五種氣體,其中可用圖2-11所示裝置制取的有.(成人高考更多完整資料免費提供加微信/QQ:29838818)
三、計算題:本題共3小題,共33分.解答時要求寫出必要的文字說明、方程式和重要的演算步驟.只寫出最后答案而未寫出主要演算過程的,不能得分.
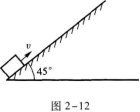
29.(本題11分)如圖2-12所示,質量為4 kg的物體以5 m/s的速度沖上斜面.斜面的傾角為45°,物體與斜面間的摩擦因數μ=0.25.求:(取g=10 m/s2.)
(1)物體能到達的最大高度;
(2)物體克服摩擦力的功.
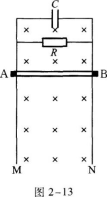
30.(本題12分)如圖2-13所示,兩根相距為l的平行的豎直金屬導軌M、N,勻強磁場垂直于導軌平面(紙面),磁感應強度為B,導軌的一端與電阻R連接,電容C與R并聯.AB為放置在導軌上的金屬棒,質量為m,棒與導軌垂直.AB的電阻為R’,導軌的電阻忽略不計.今使AB從靜止開始下滑,求:(成人高考更多完整資料免費提供加微信/QQ:29838818)
(1)AB運動的最大速度;
(2)電容器所帶的最大電荷量;
(3)電功率.
31.(本題10分)1體積水(密度為1 g/cm)吸收了560體積(標準狀況下)氨氣,所得氨水的密度為0.90 g/cm,求此溶液中溶質的質量分數.用此氨水10 mL與含7.74 g H3PO4的溶液混合,恰好完全反應,求此反應生成鹽的分子式.
物理化學模擬試卷(二)參考答案及解題指要
選擇題
一、選擇題
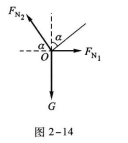
1.【參考答案】 B
【解題指要】以小球為研究對象進行受力分析.小球受三個共點力的作用:重力G,方向豎



2.【參考答案】 D
【解題指要】本題考查的知識點是勻速圓周運動和向心力的概念.
人造地球衛星做勻速圓周運動,向心力是地球對衛星的萬有引力.設衛星的質量為m,地球的質量為me,根據萬有引力公式知

ν1>ν2
選D.
3.【參考答案】 C
【解題指要】本題考查的知識點是波形圖和振動圖像.本題已知某時刻的波形圖,要求判斷介質中一個質點的振動圖像,具有一定的難度.根據t=0時的波形圖可以決定質點的初位置和初速度的方向,再與四個振動圖像中t=0時的初位置和初速度方向比較,選出正確的答案.由波形圖知,在t=0時,A點的初位置y0=0,A點的振動落后于左側的波谷,因此它向波谷運動,速度方向向下.由圖(a)見,y0=A(A為振幅),應排除.圖(b)中y0=-A,也應排除.在(c)中,ν0的方向向下,選(c).在(d)中,ν0的方向向上,也不正確.
4.【參考答案】 A
【解題指要】本題的考點是兩個電阻的并聯和滑動變阻器.
由圖2-4知,電路是固定電阻R0與滑變電阻Rx的并聯電阻.當P點滑動時,Rx變化,總電阻R隨之變化.由兩個電阻的并聯公式知
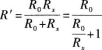

5.【參考答案】 B
【解題指要】本題的考點是左手定則和電磁感應.
先用左手定則確定線圈中感應電流的方向,再根據右手定則或楞次定律判斷線圈的運動情況.由題意知,cd所受的磁場力方向豎直向上,磁場方向垂直紙面向里,所以根據左手定則可知cd上的感應電流的方向由d到c,線圈中感應電流的流向是dcbad(順時針指向).在已知感應電流方向和磁場方向的情形下,再對da用右手定則知da的運動方向是水平向右的,選B.顯然,當線圈向上運動或向下運動時,線圈中磁通量不變,無感應電流,導線不受磁場力作用,C、D不正確.當線圈向左運動時,線圈進入磁場,感應電流的流向是逆時針方向的,dc受豎直向下的磁場力,A也不正確.
本題也可以用楞次定律解.因為閉合電路中感應電流的流向是順時針的,用右手螺旋法則知線圈中感應電流所產生的磁場方向也是垂直紙面向里的,與原磁場的方向相同.因此,根據楞次定律可知線圈在運動時通過它的磁通量是減小的,這表明線圈向右平動,離開磁場.
6.【參考答案】 D
【解題指要】由于鐵心的耦合作用,圖2-6相當于一個理想變壓器.因此,本題考查的知識點是理想變壓器,可以用變壓器公式解題.設AB之間線圈的匝數為n,由題意可知

7.【參考答案】 C
【解題指要】本題的考點是天然放射性現象的基本概念.

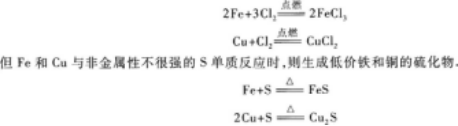
8.【參考答案】 C
【解題指要】常見的變價金屬Fe和Cu直接與非金屬單質反應時,因非金屬的氧化性強弱不同,生成不同價態的鐵和銅的化合物.如:Fe和Cu與非金屬性(即氧化性)很強的Cl2反應,生成鐵和銅的高價氯化物(嚴格地說應是在Cl2過量的條件下).
9.【參考答案】 C(成人高考更多完整資料免費提供加微信/QQ:29838818)
【解題指要】鐵是較活潑的金屬,因此可與酸和鹽等多種物質發生化學反應.例如:

10.【參考答案】 A
【解題指要】回答此題主要依據“非金屬性越強的元素,其氣態氫化物越穩定”這一規律.所以,只要知道形成氣態氫化物的非金屬元素其非金屬性的相對強弱,就可比較氣態氫化物穩定性的大小.
(1)HF、HCl、HI中,因F、Cl、I三種元素的非金屬性是由強到弱的順序,所以HF、HCl、HI的穩定性也一定是由大到小的順序.
(2)NH3、H2O、HF中,因N、O、F的非金屬性是由弱到強的順序,所以NH3、H2O、HF的穩定性是由小到大的順序.
(3)PH3、SiH4、CH4中,因非金屬性是P比Si強,但Si比C弱;H2S、HCl、HBr中,非金屬性是S比Cl弱,但Cl比Br強,所以它們的氫化物穩定性的順序既不是由大到小,也不是由小到大.
11.【參考答案】A
【解題指要】(1)用CxHy代表兩種烴組成的混合物,則可把混合物燃燒的反應方程式寫成:
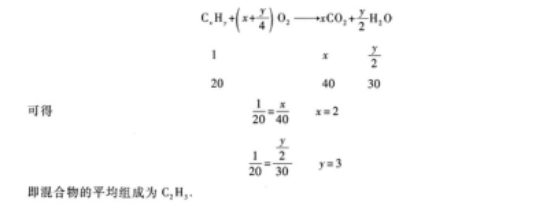
(2)組成混合物的兩種氣態烴分子中所含C、H原子數必須符合以下條件:
C原子:一個組分的C原子數小于2,另一個組分的C原子數大于2;或兩個組分的C原子數均為2.
H原子:一個組分的H原子數小于3,另一個組分的H原子數大于3;或兩個組分的H原子數均為3.
綜合考慮C原子數和H原子數,只有C2H2和C2H4符合要求.即正確選項是A.
12.【參考答案】 B
【解題指要】(1)首先根據化學方程式中化合價的變化,找出氧化劑和還原劑.
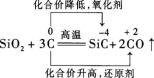
在化合物SiC中,因C的非金屬性比Si強,吸引電子的引力也比Si大,所以Si顯正價,C顯負價.
(2)計算氧化劑、還原劑的物質的量.
氧化劑、還原劑都是C.從生成物SiC的系數為1可知,反應中有1 molC原子從0價降低到-4價.同理,CO的系數為2,即有2 molC原子從0價變為+2價.也就是氧化劑為1 mol,還原劑為2 mol,還原劑與氧化劑的物質的量之比為2:1.
13.【參考答案】 C
【解題指要】本題要求在加壓或降溫兩種情況下,平衡均向右移動.解題時可逐一討論.
(1)加壓時,平衡向右移動:這要求平衡反應中氣態反應物的系數之和應大于氣態生成物的系數之和,符合此要求的只有C選項.
(2)降溫時,平衡向右移動:這要求平衡反應中正向反應是放熱反應.C選項正好也符合此要求.所以正確選項是C.
14.【參考答案】 D

15.【參考答案】 B
【解題指要】解答此題重要的是要密切結合題目的條件:

所以,得到的酸M就是HN03.
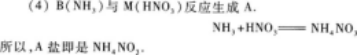
非選擇題
二、填空題
16.【參考答案】30° 1.73
【解題指要】本題的考點是光的反射定律和折射定律.
光線經過兩次折射,第一次在AB面上,第二次在AC面上,在AB面上垂直入射,入射角為零,折射角也為零.此折射光線是AC面上的入射光.它與AC面的夾角為90°-∠A=90°-30°=60°因此,AC面上光線的入射角是θi=90°-60°=30°由圖2-15知,光線在AC面上折射后的折射光(即出射光)與AC面法線的夾角(即折射角)為θi=30°+30°=60°再根據折射定律
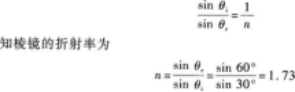
注意,考生在解題時應在圖2-7中把AC面上通過入射點的AC的垂線,即AC面的法線畫出,這樣根據幾何關系可以明確求出折射角θr(見圖2-15).
17.【參考答案】 2 10
【解題指要】本題的考點是初速度為零的勻加速直線運動.物體在光滑的斜面上受重力和斜面支持力的作用,重力和支持力的合力沿斜面向下,因此物體做勻加速直線運動.重力、支持力的合力的大小是F=mgsin θ式中θ為斜面的傾角.由牛頓第二定律知物體運動的勻加速度為
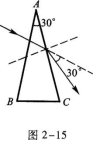
初速度為零的勻加速直線運動的位移公式是

設斜面的長度為l,物體運動到中點時的位移為

18.【參考答案】 1.41×10-2水平向右
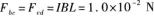
【解題指要】本題具有一定的綜合性.考查的知識點是磁場力、左手定則和力的合成.由安培力公式得用左手定則可知Fbc的方向垂直bc指向右下,Fcd的方向垂直cd指向右上,它們相互垂直,如圖2-16所示.

根據力的合成法則知,合力F的大小為

F的方向水平向右.向考生介紹一個有用的結論:一根通電折導線在勻強磁場中所受的磁場力等于由這根導線的起點引向終點的直導線所受的磁場力.在本題的情形下,折線bcd所受的磁場力等于直線bd所受的磁場力.由此可見顯然直接用此結論解本題要方便得多,無需分別計算Fbc和Fcd,再用力的合成計算F.
19.【參考答案】5 2.5 2.5

![]()
【解題指要】本題考查的知識點是用伏安法測量電源電動勢和內電阻、伏安曲線、閉合電路歐姆定律.根據閉合電路歐姆定律知
![]()
由此得電源的路端電壓為
![]()

由此可知,路端電壓與電流呈線性關系,因此U-I,曲線(伏安曲線)是直線,正如圖2-10所示.在U-I圖中,直線段斜率的絕對值等于電源的內電阻r的阻值,直線段在縱軸(U軸)上的截由圖2-10知,直線段在U軸上的截距是5 V,因此由圖可求出直線斜率的絕對值為
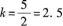
因此電源的內阻r=2.5 Ω
再由圖見,當路端電壓U=2.5 V時,電流I=1 A.根據歐姆定律

20.
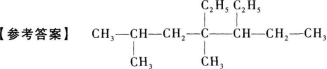
【解題指要】
(I)庚烷——最長碳鏈中應含有7個碳原子.
(2)連有取代基的碳原子上的H原子數要寫對.不連取代基的中間C原子上,應有2個H原子;連有1個取代基的C原子上,應去掉1個H原子,還有1個H原子;連有2個取代基的C原子上,應去掉2個H原子,即此C原子上沒有H原子.
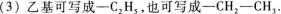
21.【參考答案】72
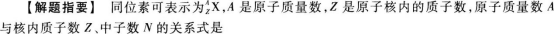
A=Z+N
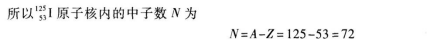
22.【參考答案】C6H10
【解題指要】此題已知烴是炔烴,故可用炔烴的通式CnH2n-2寫出燃燒反應的化學方程式,然后再進行相關計算.
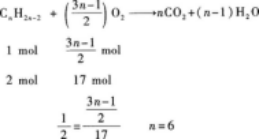
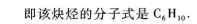
23.【參考答案】 12
【解題指要】

因此,混合后可能有以下三種情況:
①恰好完全反應.因BaCl2是強酸強堿鹽,所以溶液顯中性.
②酸有剩余,溶液顯酸性.
③堿有剩余,溶液顯堿性.
究竟屬于哪一種情況,需經計算才能知道.
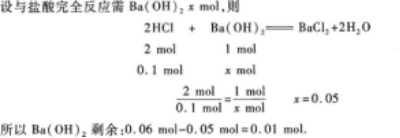
(3)計算混合后溶液的pH.
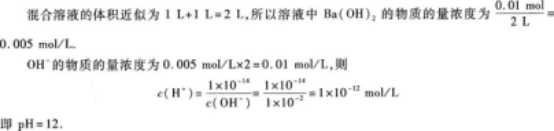
24.【參考答案】1.5
【解題指要】

反應中沒有都被氧化,所以最好根據Cl元素得到的電子數來計算.3Cl2一6Cl-這一過程,需得到6 mol電子,即反應中轉移了6 mol電子.
(2)找出轉移電子數與生成N2的體積的定量關系式:

25.【參考答案】HCHO
【解題指要】
(1)先求有機物的相對分子質量
Mr=32x0.938=30
(2)求有機物的分子式
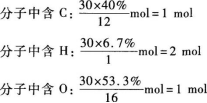
即有機物的分子式為CH2O.
(3)求有機物的結構式因分子中只含有1個0原子,所以只可能是醇類或醛類.
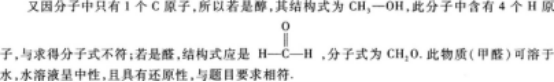

26.【參考答案】
【解題指要】
(1)向三種溶液中分別加入鹽酸并加熱.
①B溶液產生白色沉淀,說明B溶液中含有Ag+.易溶于水的銀鹽只有AgNO3,所以B物質是AgNO3.

(2)向A溶液中加入NaOH溶液.

(3)向C溶液中加入過量NaOH溶液并加熱,產生有刺激性氣味的氣體,這是NH+4的特征反應現象.所以C物質是(NH4)2CO3.所以,A物質是Al2(SO4)3,B物質是AgNO3,C物質是(NH4)2CO3.
 欧美日本一道免费一区三区,欧美日韩精品在线视频,精品久久久久久蜜臂a∨,国产99视频精品一区
99国产精品久久久|
欧美色男人天堂|
www国产精品av|
久久99在线观看|
日韩精品一区二区三区中文精品|
三级精品在线观看|
久久免费看少妇高潮|
成人在线综合网站|
一区二区三区在线视频免费观看|
欧美喷水一区二区|
懂色av一区二区在线播放|
亚洲视频一区二区在线|
制服视频三区第一页精品|
久久99热狠狠色一区二区|
国产精品免费视频网站|
欧美日韩国产一级|
成人丝袜视频网|
人人狠狠综合久久亚洲|
成人欧美一区二区三区黑人麻豆
|
91在线精品秘密一区二区|
亚洲精品五月天|
国产婷婷色一区二区三区|
欧美另类久久久品|
99国产精品久久久久久久久久久|
精品一区二区三区免费观看|
亚洲午夜在线观看视频在线|
日本一区二区不卡视频|
91精品欧美一区二区三区综合在|
色婷婷综合五月|
成人av第一页|
国产乱淫av一区二区三区|
亚洲成人精品一区|
一区在线观看视频|
中文字幕一区二区三区视频|
国产日韩精品一区二区三区|
欧美精品亚洲二区|
欧美精品aⅴ在线视频|
欧美性一区二区|
在线看日韩精品电影|
91麻豆精东视频|
91小视频免费观看|
av在线播放一区二区三区|
国产伦理精品不卡|
丁香五精品蜜臀久久久久99网站
|
欧美日本一区二区|
91久久精品一区二区二区|
欧美最猛黑人xxxxx猛交|
一本一本大道香蕉久在线精品|
91在线观看美女|
欧美在线播放高清精品|
欧美另类变人与禽xxxxx|
欧美一区二区日韩一区二区|
欧美一区二区三区喷汁尤物|
精品国产乱码久久久久久影片|
精品久久久网站|
日本一区二区三区四区在线视频|
中文字幕免费不卡|
亚洲精品ww久久久久久p站|
亚洲va韩国va欧美va精品
|
在线观看日韩国产|
欧美日韩国产成人在线免费|
91精品国产高清一区二区三区
|
国产在线精品一区二区三区不卡
|
欧美电影一区二区|
日韩一区二区三区在线观看|
精品88久久久久88久久久|
国产欧美日韩三级|
午夜精品123|
国产精品99久久久久久久vr|
91成人免费网站|
久久青草国产手机看片福利盒子|
亚洲国产精品ⅴa在线观看|
亚洲国产视频a|
国产成人免费在线观看|
欧美日韩视频第一区|
2023国产精品|
午夜视频在线观看一区二区
|
久久精品一区蜜桃臀影院|
国产日韩综合av|
蜜臀av性久久久久蜜臀av麻豆|
99久久er热在这里只有精品15|
91精品欧美久久久久久动漫
|
91在线porny国产在线看|
欧美日韩一区视频|
国产精品久久综合|
国产福利精品导航|
555夜色666亚洲国产免|
一区二区三区在线观看欧美|
国产成人免费视频网站高清观看视频|
欧美亚洲日本国产|
亚洲欧美另类久久久精品|
国产91精品在线观看|
久久综合久久综合久久综合|
青青青伊人色综合久久|
欧美综合在线视频|
亚洲一区二区三区视频在线播放|
av一区二区三区黑人|
国产午夜精品美女毛片视频|
国产一区二区三区黄视频|
日韩欧美卡一卡二|
久久激五月天综合精品|
欧美成人欧美edvon|
日本不卡一区二区三区|
欧美一区二区三区成人|
日本不卡高清视频|
精品国产一区二区三区av性色|
久久99久久久久久久久久久|
精品少妇一区二区三区免费观看
|
欧美电影影音先锋|
午夜精品久久久久久久|
欧美日韩另类国产亚洲欧美一级|
午夜亚洲国产au精品一区二区|
欧美高清精品3d|
久久精品国内一区二区三区|
精品va天堂亚洲国产|
成人美女视频在线观看|
综合分类小说区另类春色亚洲小说欧美|
成+人+亚洲+综合天堂|
亚洲欧美日韩精品久久久久|
欧美日韩一区二区三区视频|
免费在线视频一区|
欧美国产一区二区|
欧美日本视频在线|
激情久久久久久久久久久久久久久久|
久久久久久麻豆|
欧美亚洲尤物久久|
国产成人精品1024|
午夜伊人狠狠久久|
国产欧美精品日韩区二区麻豆天美|
voyeur盗摄精品|
日韩中文字幕区一区有砖一区|
337p粉嫩大胆色噜噜噜噜亚洲|
92国产精品观看|
精品系列免费在线观看|
亚洲人午夜精品天堂一二香蕉|
欧美一卡二卡在线|
色综合久久99|
国产成a人亚洲精|
蜜桃av噜噜一区|
一区二区三区日韩欧美|
国产色婷婷亚洲99精品小说|
欧美日本视频在线|
色综合久久88色综合天天免费|
国产在线国偷精品产拍免费yy|
亚洲一区二区三区四区不卡|
国产欧美日韩视频一区二区
|
日日夜夜免费精品|
欧美激情一区二区三区蜜桃视频|
欧美日韩一区二区在线视频|
国产凹凸在线观看一区二区|
日本在线不卡视频|
亚洲一区二区三区四区不卡|
最新国产成人在线观看|
久久一区二区三区四区|
日韩精品中文字幕一区|
欧美一区二区三区在线观看|
91丝袜美腿高跟国产极品老师|
韩国精品久久久|
精品无人区卡一卡二卡三乱码免费卡|
午夜亚洲国产au精品一区二区|
亚洲一二三区不卡|
一个色综合av|
亚洲成人精品一区二区|
午夜精品久久久久久久蜜桃app|
亚洲成人精品一区|
午夜成人免费电影|
日本va欧美va欧美va精品|
日韩国产欧美在线观看|
久久国产精品区|
国产成人精品免费在线|
99re热视频精品|
欧美日韩国产综合一区二区三区|
91精选在线观看|
久久久美女毛片|
国产精品对白交换视频
|
www.日本不卡|
91丝袜高跟美女视频|
色综合 综合色|
91麻豆精品国产无毒不卡在线观看|
777久久久精品|
国产欧美日韩综合精品一区二区|
**网站欧美大片在线观看|
亚洲sss视频在线视频|
精品一区二区日韩|
jiyouzz国产精品久久|
欧美性欧美巨大黑白大战|
91精品国产欧美一区二区18|
国产精品久久久久久亚洲毛片|
一个色妞综合视频在线观看|
精品一区二区三区的国产在线播放|
国产成人精品aa毛片|
欧美午夜电影网|
国产精品污网站|
日本不卡123|
色网站国产精品|
26uuuu精品一区二区|
日韩国产精品久久|
91亚洲精品久久久蜜桃|
国产欧美在线观看一区|
美女网站色91|
欧美日本一道免费一区三区,欧美日韩精品在线视频,精品久久久久久蜜臂a∨,国产99视频精品一区
99国产精品久久久|
欧美色男人天堂|
www国产精品av|
久久99在线观看|
日韩精品一区二区三区中文精品|
三级精品在线观看|
久久免费看少妇高潮|
成人在线综合网站|
一区二区三区在线视频免费观看|
欧美喷水一区二区|
懂色av一区二区在线播放|
亚洲视频一区二区在线|
制服视频三区第一页精品|
久久99热狠狠色一区二区|
国产精品免费视频网站|
欧美日韩国产一级|
成人丝袜视频网|
人人狠狠综合久久亚洲|
成人欧美一区二区三区黑人麻豆
|
91在线精品秘密一区二区|
亚洲精品五月天|
国产婷婷色一区二区三区|
欧美另类久久久品|
99国产精品久久久久久久久久久|
精品一区二区三区免费观看|
亚洲午夜在线观看视频在线|
日本一区二区不卡视频|
91精品欧美一区二区三区综合在|
色婷婷综合五月|
成人av第一页|
国产乱淫av一区二区三区|
亚洲成人精品一区|
一区在线观看视频|
中文字幕一区二区三区视频|
国产日韩精品一区二区三区|
欧美精品亚洲二区|
欧美精品aⅴ在线视频|
欧美性一区二区|
在线看日韩精品电影|
91麻豆精东视频|
91小视频免费观看|
av在线播放一区二区三区|
国产伦理精品不卡|
丁香五精品蜜臀久久久久99网站
|
欧美日本一区二区|
91久久精品一区二区二区|
欧美最猛黑人xxxxx猛交|
一本一本大道香蕉久在线精品|
91在线观看美女|
欧美在线播放高清精品|
欧美另类变人与禽xxxxx|
欧美一区二区日韩一区二区|
欧美一区二区三区喷汁尤物|
精品国产乱码久久久久久影片|
精品久久久网站|
日本一区二区三区四区在线视频|
中文字幕免费不卡|
亚洲精品ww久久久久久p站|
亚洲va韩国va欧美va精品
|
在线观看日韩国产|
欧美日韩国产成人在线免费|
91精品国产高清一区二区三区
|
国产在线精品一区二区三区不卡
|
欧美电影一区二区|
日韩一区二区三区在线观看|
精品88久久久久88久久久|
国产欧美日韩三级|
午夜精品123|
国产精品99久久久久久久vr|
91成人免费网站|
久久青草国产手机看片福利盒子|
亚洲国产精品ⅴa在线观看|
亚洲国产视频a|
国产成人免费在线观看|
欧美日韩视频第一区|
2023国产精品|
午夜视频在线观看一区二区
|
久久精品一区蜜桃臀影院|
国产日韩综合av|
蜜臀av性久久久久蜜臀av麻豆|
99久久er热在这里只有精品15|
91精品欧美久久久久久动漫
|
91在线porny国产在线看|
欧美日韩一区视频|
国产精品久久综合|
国产福利精品导航|
555夜色666亚洲国产免|
一区二区三区在线观看欧美|
国产成人免费视频网站高清观看视频|
欧美亚洲日本国产|
亚洲欧美另类久久久精品|
国产91精品在线观看|
久久综合久久综合久久综合|
青青青伊人色综合久久|
欧美综合在线视频|
亚洲一区二区三区视频在线播放|
av一区二区三区黑人|
国产午夜精品美女毛片视频|
国产一区二区三区黄视频|
日韩欧美卡一卡二|
久久激五月天综合精品|
欧美成人欧美edvon|
日本不卡一区二区三区|
欧美一区二区三区成人|
日本不卡高清视频|
精品国产一区二区三区av性色|
久久99久久久久久久久久久|
精品少妇一区二区三区免费观看
|
欧美电影影音先锋|
午夜精品久久久久久久|
欧美日韩另类国产亚洲欧美一级|
午夜亚洲国产au精品一区二区|
欧美高清精品3d|
久久精品国内一区二区三区|
精品va天堂亚洲国产|
成人美女视频在线观看|
综合分类小说区另类春色亚洲小说欧美|
成+人+亚洲+综合天堂|
亚洲欧美日韩精品久久久久|
欧美日韩一区二区三区视频|
免费在线视频一区|
欧美国产一区二区|
欧美日本视频在线|
激情久久久久久久久久久久久久久久|
久久久久久麻豆|
欧美亚洲尤物久久|
国产成人精品1024|
午夜伊人狠狠久久|
国产欧美精品日韩区二区麻豆天美|
voyeur盗摄精品|
日韩中文字幕区一区有砖一区|
337p粉嫩大胆色噜噜噜噜亚洲|
92国产精品观看|
精品系列免费在线观看|
亚洲人午夜精品天堂一二香蕉|
欧美一卡二卡在线|
色综合久久99|
国产成a人亚洲精|
蜜桃av噜噜一区|
一区二区三区日韩欧美|
国产色婷婷亚洲99精品小说|
欧美日本视频在线|
色综合久久88色综合天天免费|
国产在线国偷精品产拍免费yy|
亚洲一区二区三区四区不卡|
国产欧美日韩视频一区二区
|
日日夜夜免费精品|
欧美激情一区二区三区蜜桃视频|
欧美日韩一区二区在线视频|
国产凹凸在线观看一区二区|
日本在线不卡视频|
亚洲一区二区三区四区不卡|
最新国产成人在线观看|
久久一区二区三区四区|
日韩精品中文字幕一区|
欧美一区二区三区在线观看|
91丝袜美腿高跟国产极品老师|
韩国精品久久久|
精品无人区卡一卡二卡三乱码免费卡|
午夜亚洲国产au精品一区二区|
亚洲一二三区不卡|
一个色综合av|
亚洲成人精品一区二区|
午夜精品久久久久久久蜜桃app|
亚洲成人精品一区|
午夜成人免费电影|
日本va欧美va欧美va精品|
日韩国产欧美在线观看|
久久国产精品区|
国产成人精品免费在线|
99re热视频精品|
欧美日韩国产综合一区二区三区|
91精选在线观看|
久久久美女毛片|
国产精品对白交换视频
|
www.日本不卡|
91丝袜高跟美女视频|
色综合 综合色|
91麻豆精品国产无毒不卡在线观看|
777久久久精品|
国产欧美日韩综合精品一区二区|
**网站欧美大片在线观看|
亚洲sss视频在线视频|
精品一区二区日韩|
jiyouzz国产精品久久|
欧美性欧美巨大黑白大战|
91精品国产欧美一区二区18|
国产精品久久久久久亚洲毛片|
一个色妞综合视频在线观看|
精品一区二区三区的国产在线播放|
国产成人精品aa毛片|
欧美午夜电影网|
国产精品污网站|
日本不卡123|
色网站国产精品|
26uuuu精品一区二区|
日韩国产精品久久|
91亚洲精品久久久蜜桃|
国产欧美在线观看一区|
美女网站色91|